Окисление - это процесс, который происходит в результате взаимодействия вещества или материала с кислородом. Этот процесс имеет большое значение для жизни на Земле, так как позволяет организмам использовать химическую энергию, создавать новые соединения и разлагать старые.
Окисление может происходить как в атмосферном воздухе, так и в водной среде. В атмосфере часто встречается окисление металлов, когда они выделяются на поверхности и реагируют с кислородом, образуя оксиды. В результате этой реакции происходит образование ржавчины на металлических поверхностях.
В водной среде окисление может происходить в результате реакции между веществом и кислородом, который растворен в воде. Процесс окисления растений, например, происходит в результате фотосинтеза, когда растение использует энергию солнца для преобразования углекислого газа и воды в глюкозу. В процессе реакции кислород окисляет углекислый газ, а вода служит источником водорода для образования глюкозы.
Когда происходит процесс окисления?

Процесс окисления может происходить в различных ситуациях и условиях. Он может быть видим для нас, как в случае с ржавелой поверхностью металла или потускневшим яблоком, или может происходить незаметно, как в случае с медленным окислением пищевых продуктов.
Окисление происходит при наличии трех основных условий:
- Наличие окислителя, такого как воздух, кислород или другие химические вещества.
- Наличие вещества, которое подвергается окислению, или вещество-окисляемое.
- Наличие энергии или активатора реакции, который способствует процессу окисления.
Процесс окисления может происходить в разных сферах жизни, таких как химия, биология и геология. Он может быть полезным, как в случае с дыханием, где окисление позволяет нашим клеткам получать энергию, или может быть вредным, когда окислительные процессы вызывают повреждение тканей или разрушение материалов.
Окисление в атмосфере
Окисление в атмосфере включает в себя несколько основных процессов:
- Окисление азота. В атмосфере азот взаимодействует с кислородом при высоких температурах и давлениях, образуя оксид азота. Этот соединение играет важную роль в образовании смога и кислотных осадков.
- Окисление серы. Главным источником серы в атмосфере является сжигание ископаемого топлива. В результате окисления серы образуются оксиды серы, которые также являются основными компонентами кислотных осадков.
- Окисление углерода. Самым известным процессом окисления углерода является горение, в результате которого образуется углекислый газ. Окисление углерода также играет важную роль в биологических процессах, например, в дыхании и фотосинтезе.
Окисление в атмосфере имеет серьезные последствия для окружающей среды и человека. Образующиеся в результате окисления соединения могут вызывать загрязнение воздуха и грунтовых вод, а также оказывать вредное воздействие на здоровье человека. Поэтому контроль и снижение уровня окисления в атмосфере являются важными задачами экологической политики и промышленности.
Окисление при хранении продуктов

В результате окисления продукт может потерять свои органолептические свойства, такие как вкус, запах и текстуру. Окисленные продукты часто приобретают неприятный запах или горький привкус.
Окисление нежелательно также и по причине того, что оно может привести к образованию вредных соединений, например, свободных радикалов. Они могут влиять на клеточный уровень организма и способствовать развитию различных заболеваний.
Для предотвращения окисления продуктов необходимо принимать соответствующие меры. Один из способов – упаковка продуктов в герметичные контейнеры или использование вакуумных упаковок. Полиэтиленовая пленка также может снизить воздействие кислорода.
Также эффективным методом является хранение продуктов в холодильнике или в замороженном состоянии. Низкая температура замедляет окисление и тем самым увеличивает срок годности продукта.
Дополнительно можно добавить антиоксиданты, такие как витамин Е или аскорбиновая кислота, которые помогают уменьшить процесс окисления. Однако, важно учитывать, что они тоже могут ухудшить органолептические характеристики продукта.
Итак, окисление при хранении продуктов является неизбежным процессом, который можно замедлить, но невозможно полностью остановить. Правильное хранение и использование антиоксидантов помогут сохранить продукты в свежем и безопасном состоянии на протяжении длительного времени.
Окисление в организме
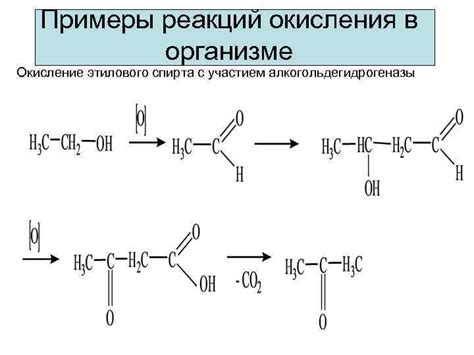
Окисление в организме осуществляется с помощью различных ферментов и молекул, таких как кислород, сера, азот и др. Основную роль в процессе окисления выполняют митохондрии – органоиды клеток, которые синтезируют большую часть энергии для клеточной деятельности.
Комплексный процесс окисления в организме состоит из нескольких этапов:
- Гликолиз – разложение глюкозы с образованием пирогрувата и небольшого количества энергии.
- Цикл Кребса (цикл трикарбоновых кислот) – дальнейший распад пирогрувата с образованием энергии в виде НАДН и ФАДННН, которые затем используются в следующем этапе.
- Окислительное фосфорилирование – ферментативный процесс, при котором образованные в предыдущих этапах энергия и электроны окислителей (НАДН и ФАДНН) используются для синтеза АТФ – универсальной молекулы энергии.
Окисление в организме является ключевым процессом в обмене веществ и обеспечивает нормальное функционирование органов и систем организма. Нарушение регуляции окислительных процессов может привести к различным заболеваниям, таким как диабет, сердечно-сосудистые заболевания и т.д.
Как происходит процесс окисления?

Окисление может протекать по разным механизмам, в зависимости от типа вещества и условий окружающей среды. Некоторые реакции окисления происходят быстро и явно видны благодаря изменению цвета или образованию газов. Другие окислительные процессы могут протекать медленно и незаметно, но все же оказывать воздействие на вещество.
Чтобы начать процесс окисления, вещество должно вступить в контакт с окислителем. Окислитель может быть в форме газа, жидкости или твердого вещества. При этом, окислитель должен быть способен отщепить электроны от вещества, которое окисляется. Эта потеря электронов приводит к изменению окисляемого вещества, которое становится окисленным.
Процесс окисления может иметь различные последствия. Некоторые окисления могут быть полезными, например, при сжигании топлива или окислении пищи в организме. Другие окисления могут быть вредными, так как могут вызвать повреждение клеток и структур живых организмов.
Важно отметить, что окисление - это обратная реакция к восстановлению, в которой вещество получает обратно потерянные электроны. Важную роль в реакции окисления-восстановления играют антиоксиданты, которые способны предотвратить или замедлить окисление вещества.
Химическая реакция окисления

В химической реакции окисления обычно участвуют вещество, которое окисляется, и окислитель. Вещество, которое окисляется, называется окислителем, а вещество, которое вступает в реакцию с окислителем, называется восстановителем. В результате этой реакции окислитель получает электроны от вещества, которое окисляется, и образует оксид или другие продукты.
Окисление может происходить в различных условиях, включая наличие кислорода, других газов и растворителей. Например, ржавление металлов является примером процесса окисления, при котором металл соединяется с кислородом из воздуха и образует оксид металла.
Окисление также может происходить при взаимодействии веществ с электрическим током, что называется электрохимической реакцией окисления. Примером такой реакции является процесс зарядки аккумулятора, где восстанавливается ион металла в электроде.
Химические реакции окисления имеют множество применений в нашей повседневной жизни. Они используются для производства электроэнергии, а также в биологических процессах, таких как дыхание и горение. Реакции окисления также играют важную роль в химической промышленности, например, в производстве стали и производстве удобрений.
Таким образом, химическая реакция окисления - это процесс обмена электронами между веществами, в результате которого происходит изменение степени окисления и образование новых продуктов.
Роль кислорода в процессе окисления
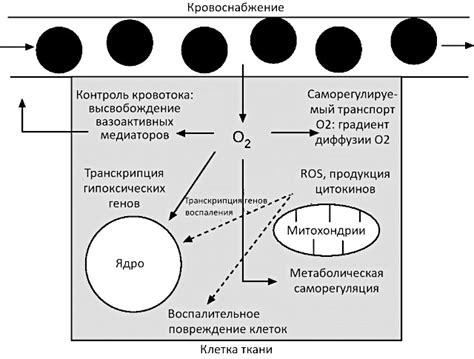
Кислород является сильным окислителем - веществом, способным отдавать электроны другим веществам. В результате окисления вещества, происходит перенос электронов со вещества на кислород. Это приводит к образованию новых химических связей, исходное вещество меняет свое строение и свойства.
Процесс окисления играет важную роль в различных аспектах жизни и природы. Например, окисление позволяет организмам получать энергию путем окисления пищи. Также окисление необходимо для дыхания - оживлено работают жизненно важные органы.
Кислород также играет важную роль в окружающей среде, приводя к образованию окислов и окислителей. Оксиды различных элементов, образующиеся в результате окисления, могут влиять на качество воздуха, воды и земли.



