Ионная связь и ковалентная полярная связь - два разных типа химических связей, которые возникают между атомами. Но когда они образуются и как они отличаются друг от друга?
Ионная связь образуется между атомами, когда один атом отдает электроны, а другой атом получает эти электроны. В результате этой передачи электронов происходит образование положительно и отрицательно заряженных ионов. В простых терминах можно сказать, что ионная связь возникает между металлическим и неметаллическим элементами.
Ковалентная полярная связь, с другой стороны, возникает, когда два атома делят пару электронов между собой. В этом случае электроны проводят время вблизи одного атома больше, чем у другого атома, создавая разницу в электронной плотности. Это приводит к образованию полярной связи.
Различие между ионной связью и ковалентной полярной связью заключается в том, как происходит передача или деление электронов между атомами. В ионной связи электроны полностью передаются от одного атома к другому, создавая положительно и отрицательно заряженные ионы. В ковалентной полярной связи электроны делятся между атомами, но с неравным временем проведения рядом с каждым атомом.
Когда ионная связь возникает, а когда образуется ковалентная полярная связь
Ионная связь образуется между атомами, когда один атом отдает электроны другому атому. В результате происходит образование ионов с противоположными зарядами - катионов и анионов. При взаимодействии катионов и анионов образуется кристаллическая структура - ионная решетка. Ионная связь обычно возникает между металлами и неметаллами, имеющими большую разность в электроотрицательности.
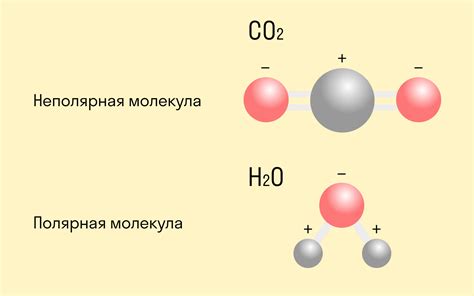
Ковалентная полярная связь образуется между атомами, когда они делят пару электронов. Однако электроотрицательности у атомов не совсем одинаковые, поэтому электроны проводимости в связи будут находиться ближе к атому с большей электроотрицательностью. Это создает неравномерное распределение зарядов и образует полярную связь. Ковалентная полярная связь чаще всего образуется между неметаллами.
Для лучшего понимания различий между этими видами связей отлично подходит таблица:
| Характеристики | Ионная связь | Ковалентная полярная связь |
|---|---|---|
| Образование | Передача электронов от одного атома к другому | Общая пара электронов с более сильно электроотрицательным атомом |
| Заряды | Образование ионов с противоположными зарядами | Неравномерное распределение зарядов |
| Типы атомов | Металлы и неметаллы с большой разностью электроотрицательности | Неметаллы с различной электроотрицательностью |
Таким образом, ионная связь образуется при передаче электронов между атомами металлов и неметаллов, имеющими большую разность в электроотрицательности. Ковалентная полярная связь возникает при общей паре электронов между неметаллами с различной электроотрицательностью.
Ионная связь в химии
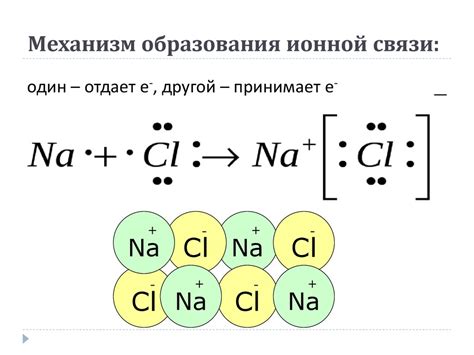
Ионная связь возникает между атомами элементов, имеющих большую разницу в электронной отрицательности. Обычно один из атомов имеет более высокую электронную отрицательность и получает электроны, становясь отрицательно заряженным ионом, а другой атом отдает электроны и становится положительно заряженным ионом.
Связь образуется благодаря электростатическому притяжению между положительными и отрицательными ионами. Ионная связь является очень сильной и обладает высокой энергией, что делает соединения, образованные ионной связью, стабильными и твёрдыми.
Примерами веществ, образованных ионной связью, являются многие соли, такие как хлорид натрия (NaCl) и нитрат калия (KNO3).
- Преобладающие свойства ионной связи:
- Высокая электроотрицательность одного из атомов;
- Высокая разница в электронной отрицательности;
- Большая разность во множестве физических и химических свойств;
- Высокая энергия связи, что делает вещество неизбирательным, твёрдым и хрупким;
- Формирование кристаллической решетки;
- Хорошая электропроводность в растворе и в расплаве, но плохая в твёрдом состоянии;
- Свойства диэлектрика.
Ионная связь имеет большое значение в химии и приложениях. Она отвечает за многочисленные физические и химические свойства веществ, а также используется в процессах синтеза, полупроводниковой технологии, оптических и электронных устройствах и в других областях науки и техники.
Ковалентная полярная связь в химии
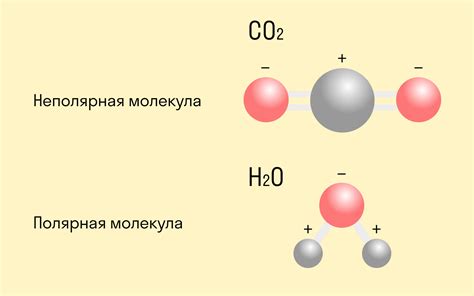
Поляризация молекулы происходит в результате различной электроотрицательности атомов, образующих связь. Электроотрицательность – это способность атома притягивать к себе общие электроны в химической связи. В случае ковалентной полярной связи, один атом оказывается сильнее электроотрицательным, чем другой, и электронная плотность смещается ближе к этому атому.
Молекула с полярной связью обладает дипольным моментом, так как электронная плотность смещена и возникает положительный и отрицательный полюс молекулы. Это может приводить к различным взаимодействиям, например, притяжению или отталкиванию, с другими молекулами.
Ковалентная полярная связь встречается в различных химических соединениях, например, в воде (H2O) или соляной кислоте (HCl). Вода образует полярную связь из-за различной электроотрицательности атомов водорода и кислорода, что приводит к положительному полюсу на водороде и отрицательному полюсу на кислороде.
Ковалентная полярная связь имеет важное значение в химической реактивности соединений. Она может влиять на реакционную способность молекулы, ее растворимость и многие другие свойства.



