Молекулы составляют основу всего материального мира и играют важную роль во всех процессах, происходящих в нем. Взаимодействие между молекулами может иметь различные последствия, в зависимости от их типа и свойств. Одним из наиболее распространенных видов взаимодействия является отталкивание.
Отталкивание между молекулами возникает в результате силы отталкивания, которая действует на растоянии между ними. Часто это происходит при приближении молекул друг к другу, когда области их электронного облака перекрываются. В такой ситуации электромагнитные силы начинают действовать, ведь электроны одной молекулы отталкивают от себя электроны другой молекулы.
Факторами, влияющими на величину отталкивающей силы, являются величины электрических зарядов частиц, их положение и расстояние между ними. Чем ближе молекулы друг к другу, тем сильнее отталкивающая сила. Также величина отталкивающей силы обратно пропорциональна расстоянию между молекулами в степени шестой. Это означает, что даже небольшие изменения расстояний могут привести к значительным изменениям величины отталкивающей силы.
Отталкивающие взаимодействия между молекулами играют важную роль в различных физических и химических процессах. Например, они могут влиять на свойства веществ, такие как плотность, вязкость и термическое расширение. Также отталкивание между молекулами может быть причиной образования защитной пленки на поверхности жидкости, что позволяет некоторым насекомым ходить по воде.
Механизм взаимодействия молекул при отталкивании
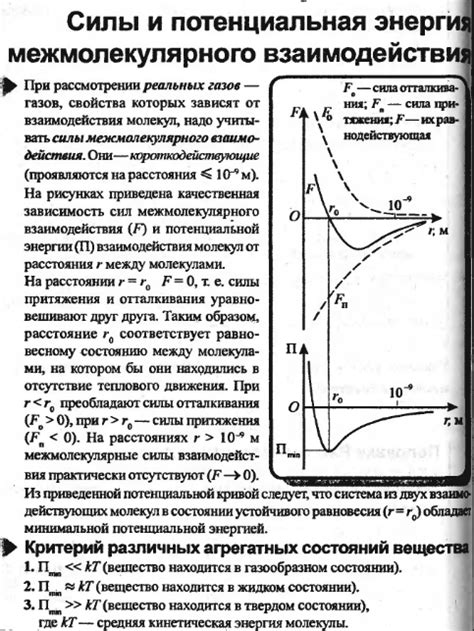
Отталкивание между молекулами происходит из-за взаимодействия их электронных облаков. Каждая молекула состоит из атомов, у которых есть электроны, движущиеся вокруг ядра. Электроны внутри молекулы образуют электронные облака, которые занимают определенные объемы.
Когда две молекулы приближаются друг к другу, их электронные облака начинают перекрываться. Заряженные частицы (электроны) в облаках начинают взаимодействовать друг с другом. Таким образом, возникают силы взаимодействия, которые стремятся вернуть молекулы в состояние равновесия.
Когда молекулы находятся на определенном расстоянии друг от друга, они начинают отталкиваться. Это происходит из-за того, что электроны, находясь в перекрывающихся облаках, начинают отталкивать друг друга, так как имеют одинаковый заряд. Соответственно, чем ближе молекулы находятся друг к другу, тем сильнее они отталкиваются.
Отталкивание между молекулами является одним из факторов, определяющих свойства вещества. Например, если молекулы сильно отталкиваются, вещество будет иметь высокую вязкость, так как молекулы трудно перемещаются друг относительно друга. Если же молекулы слабо отталкиваются, вещество будет иметь малую вязкость.
| Отличительные свойства отталкивания молекул: | Физические примеры: |
|---|---|
| Силы отталкивания возрастают с уменьшением расстояния между молекулами. | Отталкивание между молекулами в жидкостях. |
| Отталкивание между молекулами может быть электростатическим или основано на других типах сил. | Отталкивание между молекулами в газах. |
| Отталкивающие силы могут приводить к образованию положительного или отрицательного заряда на поверхности молекул. | Отталкивание между молекулами в твёрдых веществах. |
В целом, механизм взаимодействия молекул при отталкивании сложен и включает в себя различные факторы, такие как структура и заряд молекул, расстояние между ними и окружающие условия. Понимание этого механизма имеет важное значение в различных областях науки и технологий, включая физику, химию, биологию и материаловедение.
Физика отталкивания молекул

В мире молекул существует множество взаимодействий, включая притяжение и отталкивание. В этом разделе мы рассмотрим физические аспекты отталкивания между молекулами.
Отталкивание молекул является результатом электрических сил, которые возникают при приближении заряженных частичек. Когда две молекулы сближаются, их электрические поля взаимодействуют друг с другом. Если поля имеют одинаковый заряд, они начинают отталкиваться, стараясь минимизировать энергию взаимодействия.
Отталкивание между молекулами происходит не только из-за электрических сил, но и из-за других факторов, таких как наличие зарядов в молекулах или наличие магнитных свойств.
Физическое отталкивание между молекулами играет важную роль во многих аспектах естественных и химических процессов. Оно определяет свойства вещества, его агрегатное состояние и способность к образованию связей.
Изучение физики отталкивания молекул позволяет лучше понять причины различных физических явлений, а также разработать новые материалы и технологии. Например, понимание отталкивания между молекулами помогает разработать эффективные смазки, покрытия и материалы с определенными электрическими или магнитными свойствами.
Таким образом, физика отталкивания молекул играет важную роль в нашем понимании мира и является ключевым моментом в различных приложениях.
Электрические силы между молекулами
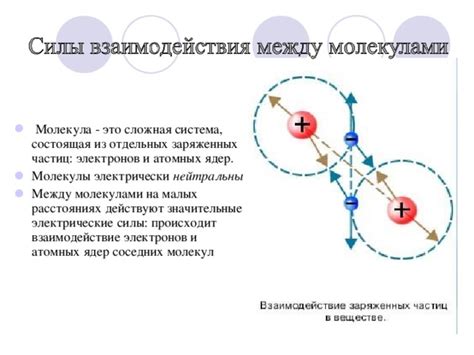
Молекулы могут обладать различными типами зарядов – положительными, отрицательными или нейтральными. При наличии зарядов возникают электрические силы притяжения или отталкивания между молекулами.
В случае, когда заряды у молекул имеют противоположный знак, возникает сила притяжения, направленная от отрицательно заряженной молекулы к положительно заряженной. Эта сила служит основой для межмолекулярных притяживающих сил, которые обеспечивают сцепление между молекулами и формирование различных структур, таких как кристаллы или жидкости.
С другой стороны, когда заряды у молекул имеют одинаковый знак, возникает сила отталкивания. Такие силы отвергают друг друга и препятствуют сцеплению молекул. Они могут быть особенно сильными, когда молекулы находятся очень близко друг к другу.
Электрические силы между молекулами играют важную роль в различных явлениях и процессах, таких как силы поверхностного натяжения, капиллярные явления и реакции сорбции. Они также являются одной из причин образования сгустков, агрегатов и структур веществ. Понимание этих сил помогает объяснить множество физических и химических свойств вещества.
Роль ван-дер-ваальсовых сил
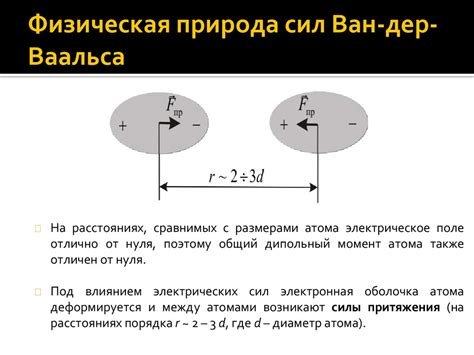
Ван-дер-ваальсовы силы особенно важны в газах и жидкостях, где они оказывают влияние на их физические свойства, например, на давление, вязкость и кипение. Кроме того, эти силы влияют на структуру и свойства многих материалов, включая полимеры, молекулярные кристаллы и биомолекулы.
Ван-дер-ваальсовы силы тесно связаны с размерами молекул и их электронной структурой. Чем больше молекулярный объем и электронная поляризуемость, тем сильнее взаимодействие. Они слабее, чем химические связи, такие как ковалентные и ионные связи, и могут быть описаны через классическую электростатику и квантовую механику.
Важно отметить, что ван-дер-ваальсовы силы действуют как притягивающие, так и отталкивающие силы между молекулами. Когда расстояние между молекулами увеличивается, возникает отталкивание, а когда расстояние уменьшается, возникает притяжение. Это отталкивание играет важную роль в определении структуры и свойств многих систем, таких как жидкости, конденсированные вещества и биологические молекулы.
Процесс отталкивания на молекулярном уровне
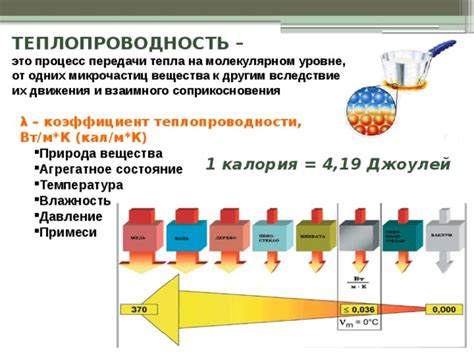
Силы отталкивания между молекулами помогают поддерживать определенное расстояние между ними. Когда две молекулы подходят друг к другу на малое расстояние, заряды на их поверхностях начинают взаимодействовать и силы отталкивания становятся сильнее.
Силы отталкивания на молекулярном уровне играют важную роль во многих физических и химических процессах. Они определяют, как молекулы будут взаимодействовать друг с другом в различных условиях. Например, в жидкостях силы отталкивания между молекулами позволяют им двигаться и располагаться в определенном порядке.
Силы отталкивания также имеют большое значение в биологических системах. Они помогают белкам и другим биологическим молекулам принимать определенную конформацию и выполнять свои функции. Благодаря силам отталкивания между молекулами клетки могут объединяться в ткани, а различные биомолекулы могут взаимодействовать, обеспечивая нормальное функционирование организма.
Необходимо отметить, что силы отталкивания не единственные силы, с которыми молекулы взаимодействуют. Существуют и другие силы, такие как силы притяжения, которые влияют на поведение молекул и на их свойства.
Понимание процесса отталкивания на молекулярном уровне является важным для различных областей науки, включая химию, физику и биологию. Исследование сил отталкивания помогает нам понять, как молекулы взаимодействуют друг с другом, и может привести к разработке новых материалов и методов в различных областях научных и технических исследований.
Роли структуры и формы молекул
Структура и форма молекул играют важную роль в их взаимодействии и проявлении отталкивания. Согласно закону отталкивания Кулона, молекулы имеют заряды, которые могут быть положительными или отрицательными. Взаимодействие молекул происходит на основе электрических сил, которые возникают из-за различия в зарядах.
Однако, чтобы эти силы срабатывали, молекулы должны быть в определенной структуре и иметь определенную форму. Структура молекул определяет расположение атомов и связей между ними, а форма молекулы определяется пространственным расположением атомов.
Структура и форма молекул влияют на следующие аспекты их взаимодействия:
| Аспект взаимодействия | Роль структуры и формы молекулы |
|---|---|
| Отталкивание между молекулами | Структура и форма молекул приводят к возникновению электрических сил отталкивания, если заряды молекул разных знаков находятся близко друг к другу. |
| Образование химических связей | Структура и форма молекулы определяют, какие атомы и в каком порядке вступают в химическую связь, что влияет на степень притяжения между молекулами. |
| Распределение зарядов на поверхности молекулы | Структура и форма молекулы определяют распределение зарядов на ее поверхности, что влияет на то, как молекулы взаимодействуют с другими молекулами и позволяет определить, является ли молекула полярной или неполярной. |
Взаимодействие молекул при проявлении отталкивания может быть сложным и зависит от множества факторов, включая не только структуру и форму молекулы, но и их размеры и энергию. Понимание роли структуры и формы молекул в этих процессах позволяет лучше понять природу взаимодействия между молекулами и их поведение в различных условиях.
Эффекты межмолекулярного отталкивания в природе

Одним из примеров эффектов межмолекулярного отталкивания является поведение жидкостей. Когда молекулы жидкости находятся очень близко друг к другу, силы отталкивания преобладают над силами притяжения, и молекулы начинают двигаться в разные стороны. Это приводит к тому, что жидкость обладает определенными свойствами, такими как форма, плотность и вязкость.
Межмолекулярное отталкивание также важно при рассмотрении воздействия насекомых на поверхности воды. У некоторых насекомых есть способность ходить по поверхности воды, благодаря различным адаптациям на молекулярном уровне. Силы отталкивания между молекулами воды и ногами насекомых создают поверхностное натяжение, что позволяет насекомым распространяться по водной поверхности без проникновения или потери устойчивости.
Кроме того, межмолекулярное отталкивание играет ключевую роль в процессах самоочищения в окружающей среде. Некоторые поверхности, такие как лотки с мыльным раствором или листья растений, обладают свойством отталкивания. Это свойство позволяет им отталкивать грязь и жидкости, что способствует самоочищению и поддержанию гигиены.



