Гидрогалогенирование – это важная реакция, которая широко используется в органической химии для получения органических соединений с галогенами. Обычно при гидрогалогенировании соблюдается правило Марковникова, согласно которому галоген добавляется к углероду, который имеет наибольшее количество водородных атомов. Однако существует класс гидрогалогенирований, при которых это правило нарушается.
Нарушение правила Марковникова может происходить, например, при гидрогалогенировании ассиметричных алкенов. В этом случае, вместо ожидаемого образования основного продукта согласно правилу Марковникова, образуется побочный продукт, где галоген добавляется к углероду с наименьшим количеством водородных атомов. Это явление может быть объяснено наличием активного места в молекуле алкена, которое привлекает галоген к себе больше, чем основное место реакции.
Нарушение правила Марковникова также возможно при гидрогалогенировании циклических алкенов. В этом случае, в отличие от гидрогалогенирования алкенов, где галоген добавляется к атому углерода, который имеет наибольшее количество водородных атомов, при гидрогалогенировании циклических алкенов галоген может добавляться к атому углерода, который имеет наименьшее количество водородных атомов. Это объясняется внутримолекулярными факторами, такими как напряжение кольца и стерические противодействия, которые могут изменять направление реакции.
Гидрогалогенирование: основное понятие

Гидрогалогенирование является одной из наиболее распространенных реакций в органической химии и широко применяется в синтезе органических соединений. При этом реакция может протекать по разным механизмам, включая радикальный, электрофильный и нуклеофильный механизмы.
Главное отличие гидрогалогенирования от других реакций добавления заключается в нарушении правила Марковникова. Правило Марковникова утверждает, что при добавлении галогена и водорода к двойной или тройной связи, атом галогена образует связь с углеродом, который уже имеет максимальное количество связей с атомами водорода. Однако в реакции гидрогалогенирования атом галогена образует связь с углеродом, не имеющим наибольшей степени замещения водородом.
Гидрогалогенирование является важным процессом при получении различных органических соединений, таких как лекарственные препараты, пластиковые материалы, пестициды и другие химические вещества. Контроль над механизмом реакции и правилом Марковникова позволяет синтезировать прекурсоры и интермедиаты со специфическими свойствами, что открывает возможности для создания новых веществ и материалов с улучшенными характеристиками.
Правило Марковникова и его значение
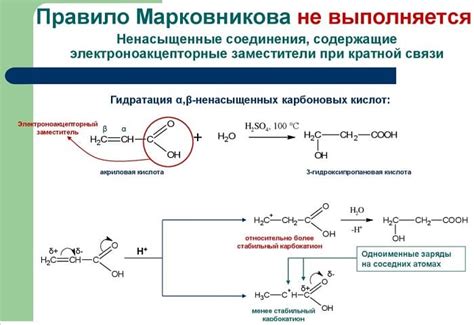
Правило Марковникова играет важную роль в реакциях гидрогалогенирования и помогает предсказывать направление присоединения атома галогена. Применение правила Марковникова позволяет определить, к какому атому углерода присоединяется галоген, что является важной информацией при изучении реакций и синтезе органических соединений.
Важно отметить, что существуют некоторые исключения из правила Марковникова, особенно при использовании радикальных реакций или когда присутствует неконъюгированный двойной связанный углерод. Однако, в большинстве случаев правило Марковникова имеет силу и используется для предсказания реакционных путей.
| Пример | Правило Марковникова | Исключение |
|---|---|---|
| CH3CH=CH2 + HBr | CH3CH2CH2Br | CH3CHBrCH3 |
| CH3CH=CHCO2H + HCl | CH3CHClCH=CHCO2H | CH3COCH2CH=CHCO2H |
Таким образом, правило Марковникова помогает химикам понять, каким образом молекулы соединений присоединяются и формируются в реакции гидрогалогенирования. Знание этого правила позволяет сделать предсказания о реакционных путях и оптимизировать синтез органических соединений.
Нарушение правила Марковникова
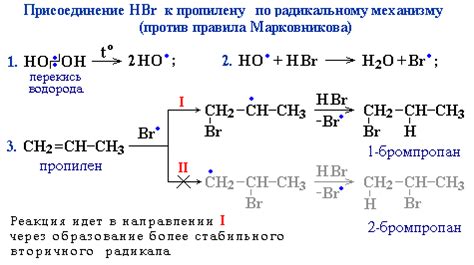
Однако, в определенных случаях, правило Марковникова может быть нарушено. Нарушение этого правила может быть вызвано различными факторами, включая кинетические эффекты, реакционные условия и стерическую доступность.
Один из примеров нарушения правила Марковникова - реакция гидрирования ацетилена. При добавлении водорода к ацетилену, гидрогалогенирование происходит анти-Марковниковским образом, то есть водород присоединяется к углероду с наибольшим числом водородных атомов, а галоген - к углероду с наименьшим числом водородных атомов.
Одной из причин нарушения правила Марковникова в реакции гидрогалогенирования является наличие катализаторов или изменение реакционных условий. Например, использование перекиси водорода вместо галогена в присутствии катализатора может привести к образованию продукта с анти-Марковниковской ориентацией.
Стерическая доступность также может быть причиной нарушения правила Марковникова. Если углерод с наибольшим числом водородных атомов занимает более затруднительное пространственное положение, чем углерод с наименьшим числом водородных атомов, галоген может присоединиться к углероду с наибольшим числом водородных атомов.
Изменение порядка добавления галогена

Обычно в гидрогалогенировании галоген добавляется к углеводороду таким образом, что один атом галогена присоединяется к атому углерода с более высокой заместительной способностью, а другой атом галогена к атому углерода с более низкой заместительной способностью. Иначе говоря, добавление галогена происходит с соблюдением правила Марковникова.
Однако в ряде случаев можно наблюдать нарушение правила Марковникова, когда галоген добавляется к углеводороду в обратной последовательности. Такое явление возможно при определенных условиях.
Изменение порядка добавления галогена может быть обусловлено присутствием вещества, которое катализирует реакцию гидрогалогенирования и может изменять механизм этой реакции. Такие вещества называются каталитическими средствами. Примером такого вещества является пероксид водорода (H2O2), которое может способствовать обратному порядку добавления галогена.
Изменение порядка добавления галогена может также происходить в условиях, когда температура реакции или концентрация реагентов превышает определенные значения. В таких условиях, реакция гидрогалогенирования может протекать с отклонением от правила Марковникова.
Необходимо отметить, что изменение порядка добавления галогена может оказывать значительное влияние на химические свойства и реакционную способность соединения. Данный факт является важным для разработки новых катализаторов и методов синтеза органических соединений.
Таким образом, изменение порядка добавления галогена в гидрогалогенировании позволяет расширить возможности органического синтеза и исследования в области механизма реакции.
Условия, при которых возможно нарушение правила Марковникова
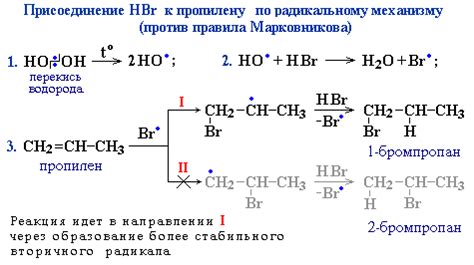
Правило Марковникова утверждает, что при гидрогалогенировании несимметричного алкена, гидроатом добавляется к тому углероду двойной связи, к которому уже присоединен наибольший количество водородных атомов. Однако существуют определенные условия, при которых это правило может быть нарушено.
Одним из таких условий является наличие каталитических агентов, которые способны изменить порядок добавления галогена. Например, при использовании перекиси водорода (Н2О2) в качестве каталитического агента, правило Марковникова может быть нарушено. В этом случае галоген будет добавляться к углероду, к которому присоединен меньший количество водородных атомов.
Еще одной причиной нарушения правила Марковникова может быть использование радикальных условий реакции. При полимеризации алкенов, например, с использованием анионных РОЛА или свободных радикалов, правило Марковникова может не соблюдаться. В этом случае гидроатом добавляется к тому углероду, к которому присоединен наибольший радикал.
Также стоит отметить, что нарушение правила Марковникова может возникнуть при реакциях, которые протекают в условиях высокого давления или при очень низкой температуре. Под воздействием таких условий происходит образование определенных промежуточных стадий реакции, которые могут привести к изменению порядка добавления галогена к алкену.
Важно отметить, что нарушение правила Марковникова на практике не является исключением, а скорее особым случаем, который требует дополнительного объяснения и понимания. Изучение условий, при которых возможно нарушение этого правила, позволяет более глубоко понять механизмы реакций гидрогалогенирования и их особенности.
Примеры реакций с нарушением правила Марковникова
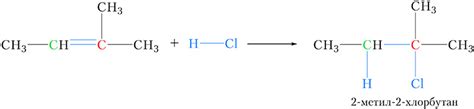
В химии существует правило, называемое правилом Марковникова, которое гласит, что в реакции гидрогалогенирования не насыщенных углеводородов, водород добавляется к углероду с большим количеством водородных атомов. Однако, есть ряд реакций, в которых это правило нарушается.
Одним из примеров является реакция гидрогалогенирования этилена или винилхлорида. По правилу Марковникова, водород должен был бы добавиться к второму углероду, у которого есть два водородных атома, но на самом деле водород добавляется к первому углероду, образуя хлорэтан:
CH2=CH2 + HCl → CH3CH2Cl
Еще одним примером является реакция гидрогалогенирования пропена. В этой реакции водород также добавляется к первому углероду вместо второго:
CH3CHCH2 + HBr → CH3CH2CH2Br
Другим примером является аддиция воды к ацетилену при наличии раствора ртути (II). В этой реакции водород и гидроксильная группа добавляются к ацетилену, образуя этанол:
C2H2 + H2O → C2H5OH
Целый ряд реакций, включая эти примеры, показывают, что правило Марковникова не всегда выполняется и могут существовать исключения из этого правила.
Значение нарушения правила Марковникова для синтеза органических соединений
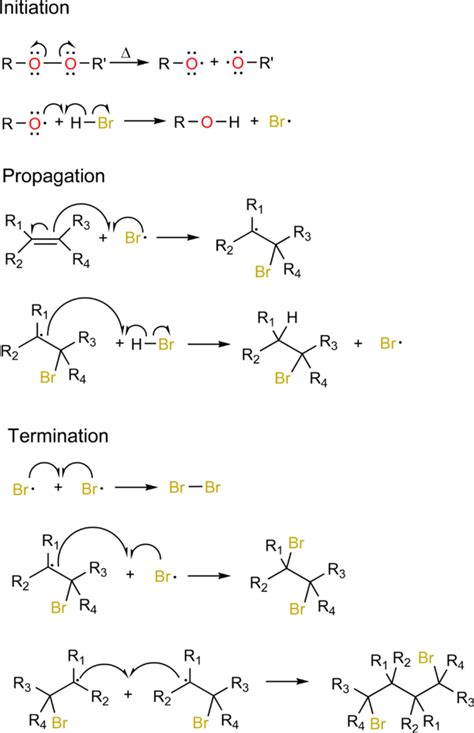
Однако, иногда в реакции гидрогалогенирования правило Марковникова может быть нарушено, в результате чего присоединение водорода происходит не к углероду с наибольшим количеством водородных атомов, а к углероду с меньшим количеством водородных атомов.
Такое нарушение правила Марковникова имеет большое значение для синтеза органических соединений, поскольку позволяет получать определенные изомеры и реагенты с нужными свойствами. Например, при синтезе антибиотиков или лекарственных препаратов, нарушение правила Марковникова может существенно повлиять на активность и эффективность получаемого продукта.
Значение нарушения правила Марковникова для синтеза органических соединений проявляется в следующих аспектах:
- Получение определенных изомеров. Нарушение правила Марковникова позволяет синтезировать изомеры с различной структурой и свойствами, что может быть важно для получения реагентов с определенными химическими и физическими свойствами.
- Управление реакцией гидрогалогенирования. Внесение изменений в условия реакции и выбор соответствующих реагентов позволяет контролировать протекание реакции и получение нужного продукта.
- Повышение активности и эффективности продукта. Нарушение правила Марковникова может привести к получению более активных и эффективных органических соединений, нежели те, которые получаются в соответствии с правилом.
- Исследование новых реакций и механизмов. Изучение нарушения правила Марковникова помогает расширить наши познания в области органической химии и разработать новые реакции и механизмы реакций.
Таким образом, нарушение правила Марковникова является важной концепцией в области синтеза органических соединений, которая позволяет управлять реакцией и получать продукты с нужными свойствами.



